Ученые создали мини-печень человека из стволовых клеток
Ученые создали биоинженерную мини-печень человека из индуцированных плюрипотентных стволовых клеток (ИПСК) и успешно трансплантировали её крысам с иммунодефицитом.
Разработка биоинженерной печени задача невероятной сложности, но она может снизить потребность в трансплантатах печени для многих пациентов циррозом, которые находятся в листах ожидания.
Ученые из Пенсильвании недавно сообщили о создании трансплантатов печени с использованием генно-инженерных индуцированных плюрипотентных стволовых клеток (ИПСК) человека, дифференцированных в клетки печени. Но биоинженерия всего трансплантата печени с использованием клеток, полученных из ИПСК человека, для трансплантации не описана.
«После трансплантации клеток мини-печени человека в организм крысы со временем она стала выглядеть, действительно как маленькая человеческая печень, и наиболее впечатляющим было то, что когда мы извлекли эту мини-печень из крыс, мы увидели, что печень выглядела по цвету и структуре как человеческая, а когда мы посмотрели на анализы крови крыс, мы обнаружили циркулирующие человеческие белки», — сообщил исследователь Алехандро Сото-Гутьеррес из Университета Питтсбурга, штат Пенсильвания.
Основным ограничением биоинженерных печеночных конструкций до сих пор была недостаточная репопуляция эндотелиальных клеток сосудистой сети, что делало их очень восприимчивыми к тромбозу, а также отсутствием других критических типов клеток, обнаруженных в печени, таких как эпителиальные клетки желчных протоков.
В текущей работе доктор Сото-Гутьеррес и его коллеги разработали протоколы дифференцировки гепатоцитов, холангиоцитов и эндотелиальных клеток ИПСК человека и высеяли децеллюляризованные каркасы печени с полученными клетками вместе с фибробластами печени и мезенхимальными стволовыми клетками для имитации микроангиоархитектоники печени.
Полученная мини-печень экспрессировала молекулы клеточного и межклеточного матриксов. Сконструированные трансплантаты печени были собранны при помощи первичных клеток печени или в трёхмерных клеточных культур, содержащих свежевыделенные первичные гепатоциты плода и взрослого человека.
Затем исследователи провели трансплантацию этой печени крысам с ослабленным иммунитетом, затем, спустя 4 дня, трансплантаты были извлечены для дальнейшей оценки.
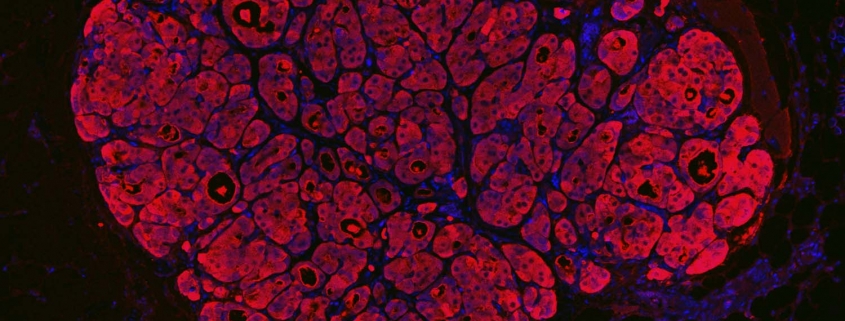
Собранные трансплантаты напоминали нормальную ткань печени, а гистологическое окрашивание показало, что гепатоциты сохранили свою морфологию и свое паренхиматозное положение. Иммуногистохимическое окрашивание подтвердило сохранение функции печени в пересаженных трансплантатах.
«Следующие шаги — это генетическая инженерия этих ИПСК для создания человеческой печени, которая будет универсальным органом в качестве трансплантата, поскольку будет минимальный риск отторжения. Опыты на крысах будут продлены, чтобы обеспечить более длительное наблюдение (в течение недель или месяцев). В планах синтезировать трансплантат для последующей имплантации свиньям», — сообщает доктор Сото-Гутьеррес. «Надеюсь, работа со свиньями будет опубликована в ближайшие месяцы. В долгосрочных планах объединить технологию ИПСК человека и создать трансплантат печени человека. Мы также должны подтвердить безопасность данного метода!»
Авторы отмечают, что до внедрения данной технологии в клиническую практику очень далеко, и это чрезвычайно сложная процедура. А стоимость массового производства и развертывания в клинике будет непомерно высокой.
«Существуют также серьезные потенциальные проблемы с плохим кровотоком и свертыванием, (и) коротким временем трансплантации, это вызывает беспокойство, будет ли такой трансплантат функционировать длительно», — сказал доктор Хэй, который не участвовал в новой работе.
У исследования не было коммерческого финансирования, но доктор Сото-Гутьеррес и некоторые из его соавторов имеют патенты, связанные с работой, и основали компанию, специализирующуюся на биотехнологии аутологичных гепатоцитов человека с использованием технологии стволовых клеток.
Источник: https://bit.ly/2Uerll2
Cell Reports, 2 июня 2020 г.



Ответить
Хотите присоединиться к обсуждению?Не стесняйтесь вносить свой вклад!